CAR-T (Chimeric Antigen Receptor T-Cell Immunotherapy),即嵌合抗原受体T细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良,并使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被认为是最有前景的肿瘤治疗方式之一。正如所有的技术一样,CAR-T技术也经历一个漫长的演化过程,正是在这一系列的演化过程中,CAR-T技术逐渐走向成熟。
这种新的治疗策略的关键之处在于识别靶细胞的被称作嵌合抗原受体(chimeric antigen receptor, CAR)的人工受体,而且在经过基因修饰后,病人T细胞能够表达这种CAR。在人体临床试验中,科学家们通过一种类似透析的过程提取出病人体内的一些T细胞,然后在实验室对它们进行基因修饰,将编码这种CAR的基因导入,这样这些T细胞就能够表达这种新的受体。这些经过基因修饰的T细胞在实验室进行增殖,随后将它们灌注回病人体内。这些T细胞利用它们表达的CAR受体结合到靶细胞表面上的分子,而这种结合触发一种内部信号产生,接着这种内部信号如此强效地激活这些T细胞以至于它们快速地摧毁靶细胞。
近年来,CAR-T免疫疗法除了被用来治疗急性白血病和非霍奇金淋巴瘤之外,经改进后,也被用来治疗实体瘤、自身免疫疾病、HIV感染和心脏病等疾病,具有更广阔的应用空间。基于此,针对CAR-T 细胞疗法取得的最新进展,小编进行一番盘点!
1.Cancer Cell:用IL-36γ武装的CAR T细胞可根除实体瘤
DOI: 10.1016/j.ccell.2025.11.007
罗斯威尔公园综合癌症中心的一项实验室研究阐述了一种新方法,能够提升嵌合抗原受体(CAR)T细胞疗法在实体瘤中的疗效,从而实现肿瘤的根除。这项研究由罗斯威尔公园综合癌症中心副主任兼医学系主任、CAR T细胞疗法领域的先驱Renier Brentjens博士领导,代表着在实体瘤领域取得与该疗法在血液恶性肿瘤中相同成功的新希望。
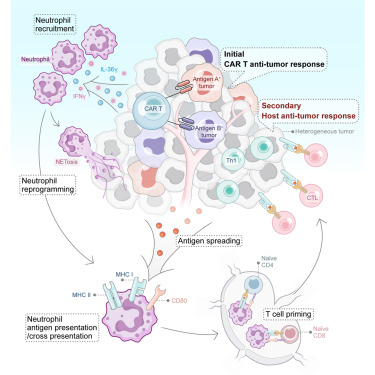
该团队(包括第一作者Yihan Zuo博士和共同资深作者Scott Abrams博士)首次证明,用细胞因子IL-36γ"武装"的CAR T细胞可以重编程称为中性粒细胞的白细胞,从而激活针对实体瘤的先天性免疫反应。他们的研究结果发表在《Cancer Cell》上。
"这项工作的激动人心之处在于,它揭示了一种新的机制,通过这种机制,CAR T细胞可以调动患者自身的免疫细胞去攻击实体瘤恶性肿瘤,"Brentjens博士表示。"我们的研究结果证实,IL-36γ CAR T细胞平台有希望成为一些目前尚无治愈方法的晚期实体瘤癌症的潜在治疗选择。"
2.PNAS:新研究开发出一种适用于所有胰腺癌的CAR-NKT细胞免疫疗法
DOI: 10.1073/pnas.2517786122
胰腺癌是最致命的癌症形式之一,大多数患者在癌细胞已扩散至全身后才被确诊。转移性病例的五年生存率仅为2-3%,中位生存期通常以月而非年计算。
如今,加州大学洛杉矶分校的研究人员开发了一种新型免疫疗法,为这种数十年来一直顽固抵抗治疗进展的疾病带来了新希望。在发表于PNAS杂志的研究中,该团队详细介绍了这种名为CAR-NKT细胞疗法的新方法,它能够在胰腺肿瘤即使已转移至其他器官后,仍能追踪并摧毁它们。
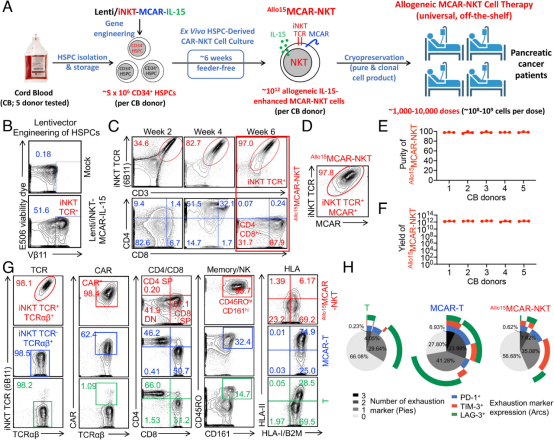
"在临床前研究中开发出一种既能靶向原发性肿瘤又能靶向其转移灶的疗法——并且是一种可以'现货供应'的疗法,代表了我们对这种疾病治疗方式的根本性转变,"该研究的资深作者、微生物学、免疫学与分子遗传学教授、加州大学洛杉矶分校再生医学与干细胞研究中心的成员Lili Yang博士表示。
该疗法使用经过工程改造的免疫细胞,这些细胞可以从捐赠的造血干细胞中大规模生产并储存备用。这种方法提供了一个立即可用的治疗选择,每剂成本约为5000美元——这仅是当前个性化细胞疗法成本的一小部分,后者可能高达数十万美元,并且需要数周的制造时间,而许多胰腺癌患者根本等不起。
3.Circulation:新型CAR-T细胞疗法可将动脉粥样硬化斑块减少70%
DOI: 10.1161/CIRCULATIONAHA.125.073987
一项开创性的临床前研究表明,CAR T细胞疗法——一种用于癌症治疗的个性化免疫疗法,可能成为对抗动脉粥样硬化的高效工具。动脉粥样硬化是指动脉中斑块积聚导致血流减少,进而引发心脏病发作和中风的病症。

在小鼠测试中,实验性的CAR T细胞阻断了动脉中的炎症,防止了超过三分之二的斑块积聚。这项由宾夕法尼亚大学佩雷尔曼医学院科学家领导的研究发表在《循环》杂志上。
"我们的研究首次展示了如何利用CAR T细胞技术来治疗最常见心脏病形式的根本原因,这种疾病是全世界范围内的主要死亡原因。这一临床前发现代表了CAR T细胞疗法在向癌症以外的常见疾病扩展影响力方面迈出的重要一步,"该研究的资深作者、药理学助理教授Avery Posey博士说。
4.Nature子刊:定制的蛋白质受体帮助T细胞更有效地靶向实体瘤
DOI: 10.1038/s41551-025-01532-3
癌症免疫疗法,尤其是利用T细胞的疗法,在治疗血癌方面展现出巨大潜力。经过生物工程改造的T细胞,特别是装备了嵌合抗原受体的CAR-T细胞,已经彻底改变了癌症治疗格局。然而,尽管它们在对抗某些血癌方面取得了显著成果,但在应对实体瘤(如乳腺癌、肺癌和前列腺癌)方面却收效甚微。

一个主要障碍是肿瘤微环境,这是一个由多种细胞和分子组成的混合体,能够抑制免疫反应。在大多数实体瘤中,抑制性信号占据主导,而有益的刺激性信号则微弱或完全缺失。由于工程化T细胞的活性和功能依赖于这些环境信号,它们往往难以发挥作用。这促使科学家们探索为T细胞构建额外受体的方法,使其能够接收肿瘤特异性信号并做出更强有力的反应。
研究人员曾尝试创建能够感知并对TME做出反应的受体,但设计过程非常困难,因为构建定制的信号蛋白是一项复杂的任务。同时,目前大多数方法严重依赖试错,这最终使得人们难以控制这些合成受体在对抗肿瘤时的实际行为。
如今,由洛桑联邦理工学院的Patrick Barth和洛桑大学/沃州大学医院的Caroline Arber领导的团队,开发了一个从头设计合成蛋白受体的计算平台。这些被称为T-SenSERs的受体,经过工程化改造,能够检测肿瘤中存在的可溶性信号,并将其转化为共刺激信号或细胞因子样信号,从而增强T细胞活性。当与传统的CAR-T细胞结合使用时,这些合成受体在肺癌和多发性骨髓瘤模型中增强了其抗肿瘤效果。这项研究发表在《自然·生物医学工程》杂志上。
5.Nature子刊:局部IL-12递送增强CAR-T细胞在实体肿瘤中的安全性
DOI: 10.1038/s41551-025-01508-3
一项由伦敦帝国理工学院和加州大学洛杉矶分校等研究人员组成的国际团队,开发出一种胶原蛋白结合型白细胞介素12策略。该策略能让CAR-T细胞治疗小鼠前列腺癌,同时抑制先前遇到的细胞因子相关毒性。
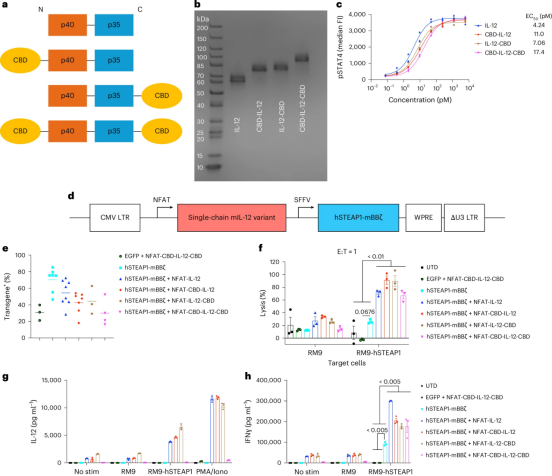
在这项发表于《自然·生物医学工程》的研究《胶原结合型IL-12增强的STEAP1 CAR-T细胞在小鼠模型中降低毒性并治疗前列腺癌》中,研究人员对靶向细胞蛋白STEAP1的CAR-T细胞进行了工程化改造,使其分泌一种与冯·维勒布兰德因子A3胶原结合结构域融合的IL-12变体,旨在将IL-12锚定在肿瘤基质内,从而降低其全身暴露。
单链IL-12变体在其N端、C端或两端携带了冯·维勒布兰德因子A3胶原结合结构域。这使得IL-12能够系留在肿瘤基质内的胶原蛋白上,限制其扩散,并将细胞因子活性集中在局部肿瘤环境中。
结果显示,在体外实验中,用这种IL-12增强的STEAP1 CAR-T细胞增加了对hSTEAP1阳性靶细胞的裂解,并提升了IFNγ水平。在小鼠肿瘤模型中,携带单个胶原结合结构域的IL-12增强的CAR-T细胞延缓了肿瘤生长,并在部分小鼠中产生了完全缓解。与胶原结合结构域融合的IL-12在瘤内水平更高,而在血清中水平更低,这与IL-12在肿瘤内的滞留和脱靶泄漏减少相一致。
6.Nature:利用CELLFIE平台有望改善CAR-T细胞疗法
DOI: 10.1038/s41586-025-09507-9
CAR T细胞是源自患者、经过基因工程改造的免疫细胞。它们作为"活体药物",堪称现代医学的里程碑。通过为免疫系统的关键细胞类型——T细胞装备"嵌合抗原受体(CAR)",使其能够特异性识别并攻击癌细胞。
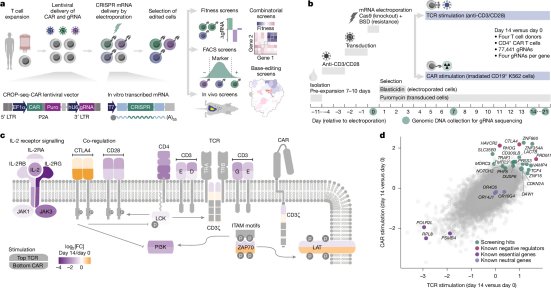
CAR T细胞疗法已通过治愈其他方法无法治疗的血癌患者证明了其潜力。但它对大多数患者仍然无效,这通常源于T细胞固有的功能障碍。为了解决当前局限并从根本上增强CAR T细胞,奥地利科学院分子医学研究中心和维也纳医科大学的科学家开发了一种系统性发现CAR T细胞功能遗传增强因子的新方法。
这项发表于《自然》杂志的新研究引入了CELLFIE——一个CAR T细胞工程化及高内涵CRISPR筛选平台,使研究人员能够系统化改造CAR T细胞并评估其治疗潜力。
"我们的CELLFIE平台可并行测试所有人类基因的敲除效果,并评估哪些基因能使CAR T细胞适应性更强、更持久或更不易耗竭,"该研究的第一作者兼共同指导者、现任美国加利福尼亚州Arc研究所组长的Paul Datlinger解释道。这导致了一个令人惊讶的遗传靶点的发现:在临床前模型中,敲除RHOG基因能显著增强CAR T细胞对抗白血病的效力。
7.Nature:体内CRISPR筛选技术有望改善CAR-T细胞的疗效
DOI: 10.1038/s41586-025-09489-8
在一项新的研究中,麻省总医院布莱根健康联盟和布罗德研究所的研究人员已识别出能够提升嵌合抗原受体T细胞疗法(CAR-T细胞)疗效的基因修饰方案。这项发表于《自然》杂志的研究通过CRISPR筛选技术,精准定位了在细胞培养物和多发性骨髓瘤临床前模型中影响T细胞功能与存活的关键基因。
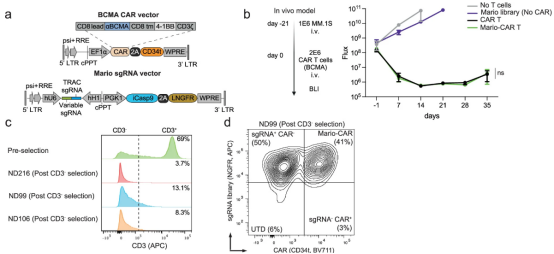
"我们针对T细胞的整个生命周期进行了筛选,将其与癌细胞共同培养,并进一步将细胞移植到动物模型中验证,"共同资深作者、麻省总医院Krantz家族癌症研究中心研究员、博德研究所肿瘤免疫治疗发现引擎主任Robert Manguso博士表示,"我们发现了在体内环境中的重要调控因子,这些是无法通过体外实验结果预测的。"
共同资深作者、麻省总医院布莱根健康联盟细胞免疫治疗项目主任、博德研究所癌症项目副成员Marcela Maus医学博士补充道:"若通过单独测试基因修饰来筛选增强CAR-T功能的靶点将耗费巨大时间和成本。我们的方法可同步检测数百种基因修饰的效果。"
本研究团队开发了一种CRISPR筛选平台,针对人类供体来源的CAR-T细胞中的135个基因进行编辑,以识别可能增强细胞持久性和功能的靶点。研究人员先将经过CRISPR编辑的细胞进行体外培养,随后移植到多发性骨髓瘤小鼠模型中,并持续追踪其21天内的体内存活情况。
他们的分析显示,删除细胞周期调控基因CDKN1B可显著提升CAR-T细胞的增殖能力、长期存活率及抗肿瘤活性。研究还观察到,部分基因仅影响体外功能而不作用于体内环境,而某些基因虽能促进肿瘤微环境中的早期增殖,却无法带来长期获益。
8.Cell:一种保护性涂层有望让通用型CAR-T细胞疗法成为可能
DOI: 10.1016/j.cell.2025.07.046
在一项新的研究中,北京大学科学家团队研发出一项癌症疗法,有望让任何地方的患者都能获得拯救生命的治疗。这种新型癌症疗法,可使更多患者获得先进治疗。该研究发表于《细胞》杂志。
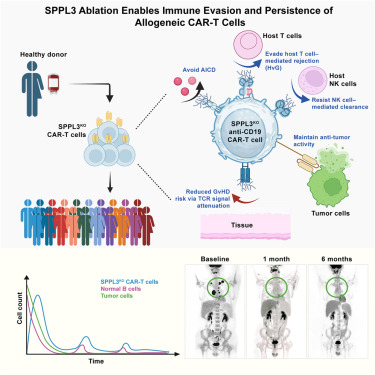
他们通过敲除单个基因,为供体CAR-T细胞赋予了类似盔甲的保护性涂层。这种涂层能帮助细胞躲避患者免疫系统的攻击,避免被清除,从而延长存活时间。在实验室测试和早期临床试验中,这种改良细胞杀伤癌细胞的效力与常规CAR-T细胞相当。更重要的是,它们能在患者体内存留数月且不引发危险副作用。
具体而言,该团队发现,敲除信号肽肽酶样3(SPPL3)可在原代T细胞中实现聚糖介导的免疫逃逸。SPPL3缺失改变了T细胞的聚糖谱,限制了配体可及性,在不影响抗CD19 CAR分子功能的前提下降低了同种异体免疫反应。
9.Science:人工智能设计的T细胞受体替代品或可加速精确的癌症免疫治疗
DOI: 10.1126/science.adv0185
借助人工智能(AI)工具设计的新型蛋白质,能够选择性靶向与病变癌细胞标记物结合的肽段,其作用类似于分子旗帜,可指示免疫细胞攻击并消灭这些威胁。
近期,一支美国研究团队取得突破性进展,成功研发出能特异性识别11种不同pMHCI复合物中肽段的蛋白质结合剂。pMHCI是存在于人体几乎所有细胞表面的氨基酸片段,在免疫系统识别和响应异常或病变细胞(如癌细胞)的过程中发挥核心作用。根据发表在《科学》杂志上的研究结果,这些通过AI设计的蛋白质可帮助人类免疫细胞更精准地识别靶标并提升免疫功能。

T细胞作为白细胞的一种,是免疫系统的前线卫士,持续监测疾病信号。它们通过扫描细胞表面的pMHCI复合物实现这一功能。当任何肽段发出异常或疾病信号时,T细胞受体(TCR)会立即识别并启动免疫细胞大军摧毁异常细胞。
由于pMHC复合物能帮助免疫系统区分感染细胞与健康细胞,这种特异性靶向能力有望革新精准治疗方法。然而,由于成本和时间限制,发现识别疾病特异性肽段所需的天然TCR面临巨大挑战。此外,鉴于人类遗传多样性,需要建立包含数十万种TCR的库才能确保广泛的患者覆盖率,并避免治疗过程中可能引发毒性的意外相互作用。
10.Cell:利用人工智能驱动的蛋白质设计来增强基于T细胞的免疫疗法
DOI: 10.1016/j.cell.2025.07.009
一篇发表于《细胞》期刊的论文重点介绍了研究人员如何利用基于人工智能(AI)的计算蛋白质设计,创造出一种新型合成配体来激活Notch信号通路——这是T细胞发育和功能的关键驱动因素。
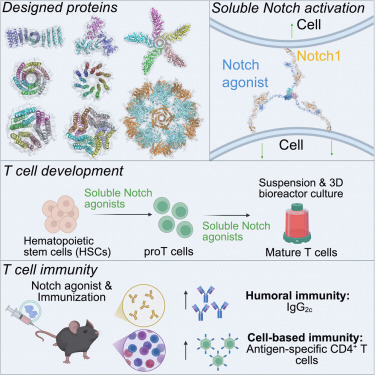
这些所谓的可溶性Notch激动剂可广泛应用于优化临床T细胞生产和推进免疫疗法开发。Notch信号是许多细胞分化过程的核心,对于将人类免疫细胞转化为靶向病毒和肿瘤的T细胞至关重要。但在实验室中激活Notch信号一直是个挑战。
为解决这一问题,哈佛医学院院长、波士顿儿童医院干细胞与再生生物学项目联合创始人George Daley实验室的研究人员及其合作者,致力于设计一种可溶性Notch激动剂,以在液体悬浮培养而非平面的二维表面上促进T细胞生产。
团队利用了计算蛋白质设计的最新进展,采用David Baker实验室开发的Rosetta蛋白质设计工具,该工具能够从头设计蛋白质。
波士顿儿童医院研究员、Baker实验室前博士后Rubul Mout与Daley实验室的同事筛选了一系列具有不同几何结构和配体呈现方式的多价Notch配体,并测试了它们的受体激活能力。他们发现反式结合构型最能促进Notch突触形成,细胞连接处的受体簇为放大的Notch激活提供了"信号枢纽"。(生物谷Bioon.com)
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
 NGS杂交捕获DNA探针 QuarStar 94基因泛肿瘤Panel 3.0 QuarStar 176基因泛肿瘤Panel 3.0 QuarStar 227基因融合Panel 1.0 QuarStar 515基因泛肿瘤Panel 1.0 杂交捕获RNA探针 人全外显子组探针3.0 HRD panel 建库试剂 DNA建库试剂盒 片段化试剂 磁珠法捕获mRNA试剂盒 rRNA去除试剂盒 QuarPro T4连接酶 杂交捕获试剂 DNA探针快速杂交捕获试剂 DNA探针杂交捕获试剂V2版 DNA探针杂交捕获试剂 RNA探针一管式过夜杂交试剂 RNA探针快速杂交捕获试剂 接头体系 封闭液系统 扩增子NGS BRCA超多重引物 超多重PCR试剂盒2.0 PathoSeq 450病原库 配套试剂 链霉亲和素磁珠 设备与软件 iQuars 50自动化工作站
NGS杂交捕获DNA探针 QuarStar 94基因泛肿瘤Panel 3.0 QuarStar 176基因泛肿瘤Panel 3.0 QuarStar 227基因融合Panel 1.0 QuarStar 515基因泛肿瘤Panel 1.0 杂交捕获RNA探针 人全外显子组探针3.0 HRD panel 建库试剂 DNA建库试剂盒 片段化试剂 磁珠法捕获mRNA试剂盒 rRNA去除试剂盒 QuarPro T4连接酶 杂交捕获试剂 DNA探针快速杂交捕获试剂 DNA探针杂交捕获试剂V2版 DNA探针杂交捕获试剂 RNA探针一管式过夜杂交试剂 RNA探针快速杂交捕获试剂 接头体系 封闭液系统 扩增子NGS BRCA超多重引物 超多重PCR试剂盒2.0 PathoSeq 450病原库 配套试剂 链霉亲和素磁珠 设备与软件 iQuars 50自动化工作站 RNA合成sgRNA miRNA siRNA
RNA合成sgRNA miRNA siRNA



 引物与探针
引物与探针 基因合成
基因合成 寡核苷酸池
寡核苷酸池 CRISPR sgRNA定制文库
CRISPR sgRNA定制文库 抗体库
抗体库 突变体库
突变体库












 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱: 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱:







