本研究通过自主构建的人源类器官肿瘤移植系统,证实肿瘤微环境中的PTPRZ1以非催化方式驱动胶质母细胞瘤间充质转化及肿瘤微管延伸,为该恶性脑癌提供全新治疗靶点与实验模型。

胶质母细胞瘤被称为“脑癌之王”,其恶性程度极高,患者确诊后平均生存期仅12至18个月,5年生存率不足6%,术后复发率更是近乎100%。长期以来,肿瘤微环境与肿瘤细胞之间的复杂通讯机制,是制约胶质母细胞瘤研究取得突破的核心难题。传统实验模型要么难以模拟人体真实的微环境,要么操作繁琐、耗时耗力,导致潜在治疗靶点的研发屡屡陷入瓶颈。
近日,发表在Cell Rep的一项研究成功打破了这一困境,研究团队通过自主开发的人源类器官肿瘤移植系统,首次揭开了肿瘤微环境中PTPRZ1蛋白调控胶质母细胞瘤进展的独特机制,为攻克这一顽疾带来全新希望。
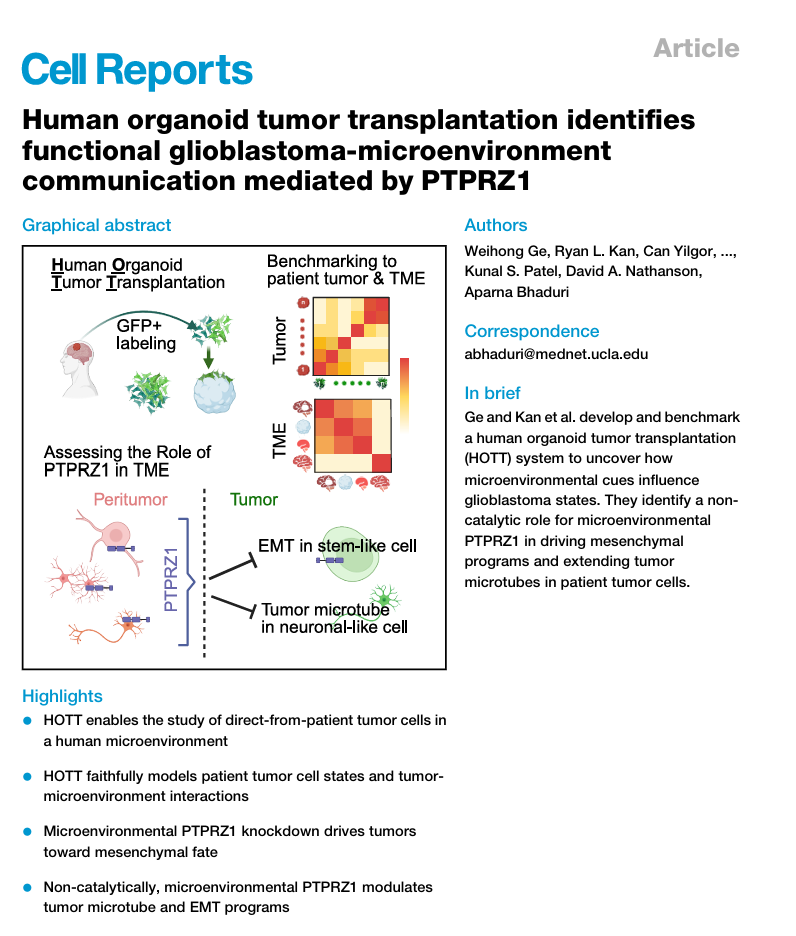
研究团队打造的人源类器官肿瘤移植系统的最大亮点在于采用直接来自患者或异种移植模型的肿瘤细胞。这些细胞未经过非脑环境的体外培养,完整保留了原发肿瘤的细胞异质性与基因特征。系统以人胚胎干细胞来源的皮质类器官为载体,构建出神经细胞富集的肿瘤微环境。
经验证,该微环境在细胞组成、分子特征、代谢基因程序及细胞间相互作用等方面,均与患者体内肿瘤微环境高度吻合。与传统胶质瘤干细胞培养模型相比,该系统能更精准重现患者肿瘤的复杂性,包括染色体7扩增、染色体10缺失等标志性基因变异,且在不同培养基条件下,均能稳定维持肿瘤干细胞样细胞及成熟细胞类型。
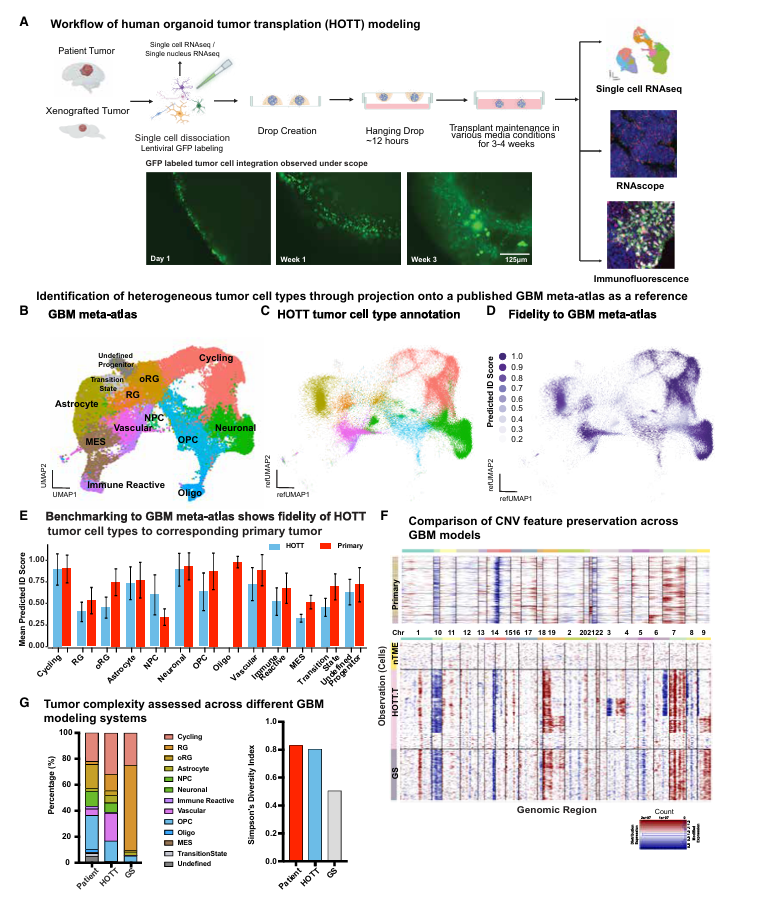
图1:人源类器官肿瘤移植来源的肿瘤细胞重现原发肿瘤特征
为解析肿瘤与微环境的通讯机制,研究团队通过专业工具分析配体-受体相互作用,筛选出在患者肿瘤与人源类器官肿瘤移植系统中均保守的四个候选基因,分别是PTPRZ1、NCAM1、MDK及CD99。这些基因均与肿瘤粘附、迁移或增殖相关,但此前它们在肿瘤微环境中的具体功能尚未明确。
研究人员在人源类器官肿瘤移植系统中对这四个基因进行短发夹RNA介导的敲低实验。结果显示,仅PTPRZ1敲低会引发肿瘤细胞的显著表型改变,其余基因敲低未导致肿瘤细胞类型出现统计学上的显著变化,这表明PTPRZ1是调控肿瘤-微环境通讯的核心因子。
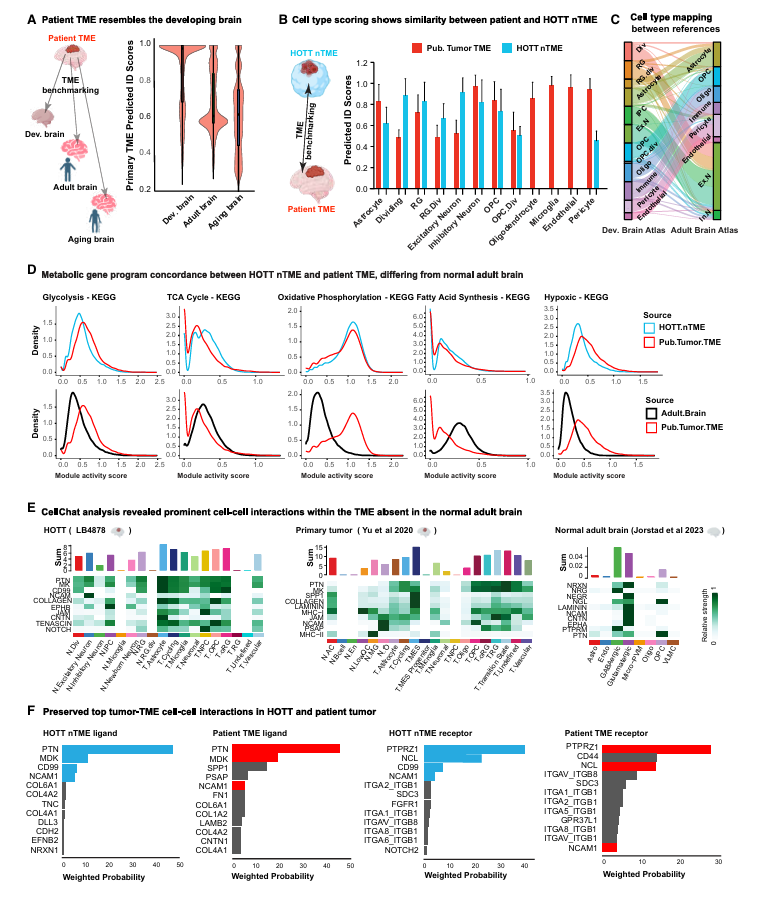
图2:人源类器官肿瘤移植系统重现患者肿瘤微环境特征
进一步研究发现,当肿瘤微环境中的PTPRZ1被敲低后,三类患者来源的肿瘤细胞均出现一致的表型变化。间充质细胞比例显著增加,混合血管细胞亚群富集,同时过渡态细胞比例显著降低。免疫荧光验证结果显示,径向胶质细胞和增殖细胞标志物SOX2、Ki67、HOPX的表达水平明显下降。
基因本体分析表明,PTPRZ1敲低显著上调了所有肿瘤细胞及干细胞样细胞中的上皮-间质转化基因程序,且这些上皮-间质转化基因与细胞迁移功能高度相关。与此同时,肿瘤微管长度显著延长。肿瘤微管作为胶质瘤细胞形成的互连网络结构,是肿瘤侵袭和迁移的关键结构基础,其长度变化直接反映肿瘤的侵袭能力。
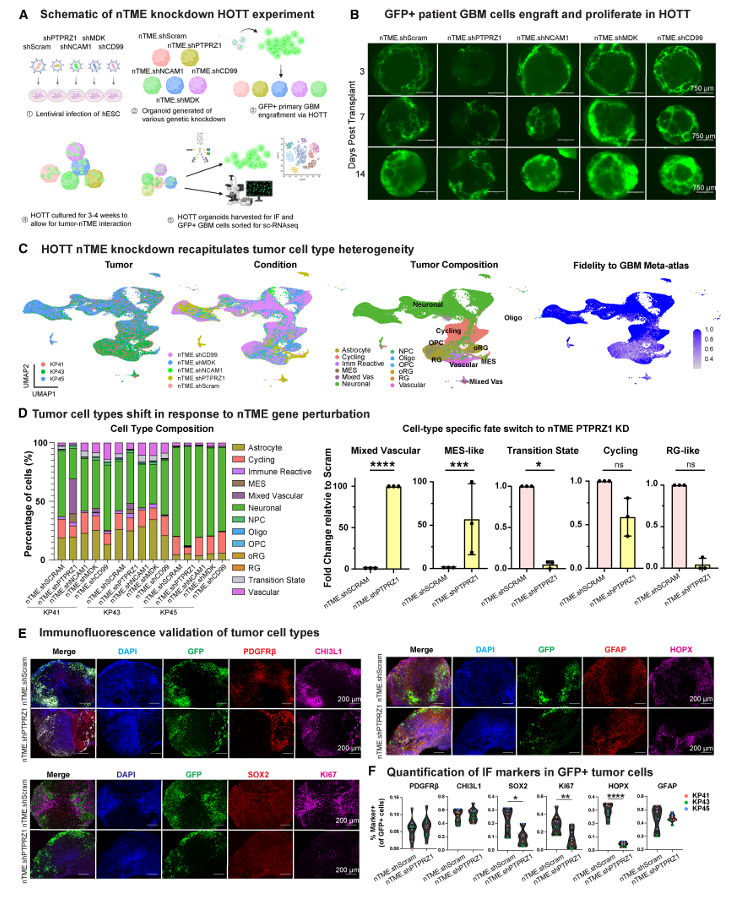
图3:人源类器官肿瘤移植系统捕捉肿瘤微环境基因扰动驱动的肿瘤细胞类型转变
PTPRZ1作为受体酪氨酸磷酸酶,传统观点认为其通过催化去磷酸化作用调控肿瘤细胞内在功能。但本研究得出了意外发现,使用PTPRZ1催化抑制剂NAZ2329处理后,并未重现PTPRZ1敲低引发的肿瘤细胞表型变化。这表明PTPRZ1调控肿瘤细胞命运的作用不依赖其催化活性,而是通过细胞间通讯实现。
深入分析显示,PTPRZ1与配体PTN在肿瘤核心区和边缘区的肿瘤细胞及非肿瘤细胞中均共同表达,构成关键信号轴,调控肿瘤间充质样细胞和混合血管细胞群的通讯。此外,PTPRZ1敲低还能显著减少肿瘤负荷,这一发现为治疗干预提供了潜在切入点。
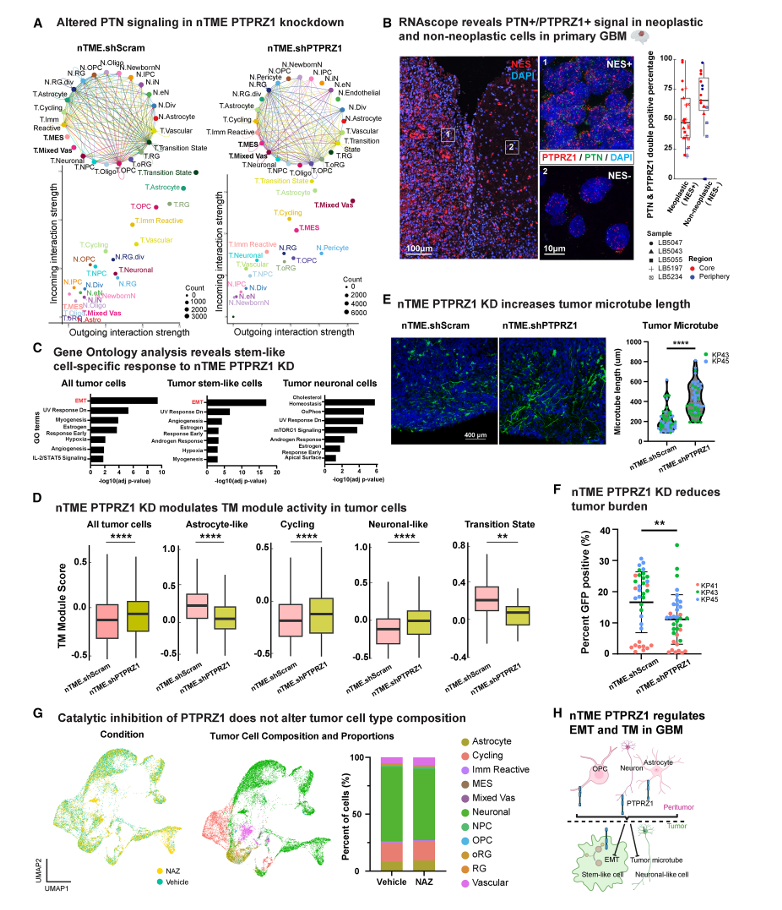
图4:肿瘤微环境中PTPRZ1敲低驱动肿瘤上皮-间质转化
综上,这项研究通过创新的人源类器官肿瘤移植系统,成功突破了传统模型的局限,首次揭示了肿瘤微环境中PTPRZ1的非催化功能。该蛋白作为细胞间通讯介质,在调控胶质母细胞瘤间充质转化、肿瘤微管形成及肿瘤负荷方面发挥关键作用。这一发现不仅丰富了人类对肿瘤-微环境相互作用的认知,更提供了全新的治疗靶点与精准的实验工具。未来,基于这一发现开发的靶向疗法,有望精准干预肿瘤微环境通讯,为改善胶质母细胞瘤患者的治疗结局、提升生存质量带来新的突破,也为恶性肿瘤的微环境靶向治疗研究提供重要参考。(生物谷Bioon.com)
参考文献:
Ge W, Kan RL, Yilgor C, et al. Human organoid tumor transplantation identifies functional glioblastoma-microenvironment communication mediated by PTPRZ1. Cell Rep. Published online January 14, 2026. doi:10.1016/j.celrep.2025.116848
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
 NGS杂交捕获DNA探针 QuarStar 94基因泛肿瘤Panel 3.0 QuarStar 176基因泛肿瘤Panel 3.0 QuarStar 227基因融合Panel 1.0 QuarStar 515基因泛肿瘤Panel 1.0 杂交捕获RNA探针 人全外显子组探针3.0 HRD panel 建库试剂 DNA建库试剂盒 片段化试剂 磁珠法捕获mRNA试剂盒 rRNA去除试剂盒 QuarPro T4连接酶 杂交捕获试剂 DNA探针快速杂交捕获试剂 DNA探针杂交捕获试剂V2版 DNA探针杂交捕获试剂 RNA探针一管式过夜杂交试剂 RNA探针快速杂交捕获试剂 接头体系 封闭液系统 扩增子NGS BRCA超多重引物 超多重PCR试剂盒2.0 PathoSeq 450病原库 配套试剂 链霉亲和素磁珠 设备与软件 iQuars 50自动化工作站
NGS杂交捕获DNA探针 QuarStar 94基因泛肿瘤Panel 3.0 QuarStar 176基因泛肿瘤Panel 3.0 QuarStar 227基因融合Panel 1.0 QuarStar 515基因泛肿瘤Panel 1.0 杂交捕获RNA探针 人全外显子组探针3.0 HRD panel 建库试剂 DNA建库试剂盒 片段化试剂 磁珠法捕获mRNA试剂盒 rRNA去除试剂盒 QuarPro T4连接酶 杂交捕获试剂 DNA探针快速杂交捕获试剂 DNA探针杂交捕获试剂V2版 DNA探针杂交捕获试剂 RNA探针一管式过夜杂交试剂 RNA探针快速杂交捕获试剂 接头体系 封闭液系统 扩增子NGS BRCA超多重引物 超多重PCR试剂盒2.0 PathoSeq 450病原库 配套试剂 链霉亲和素磁珠 设备与软件 iQuars 50自动化工作站 RNA合成sgRNA miRNA siRNA
RNA合成sgRNA miRNA siRNA



 引物与探针
引物与探针 基因合成
基因合成 寡核苷酸池
寡核苷酸池 CRISPR sgRNA定制文库
CRISPR sgRNA定制文库 抗体库
抗体库 突变体库
突变体库








 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱: 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱:







